
дата |
тема |
к чему стремиться |
к уроку |
домашнее задание |
10.09 |
Объёмные отношения газов при химических реакциях | Основные понятия: Закон Авогадро, молярный объём |
5 задач на выбор |
Теоретический материал
Объёмы реагирующих и образующихся газов, измеренные при одинаковых условиях, относятся как небольшие целые числа (коэффициенты в уравнении реакции)
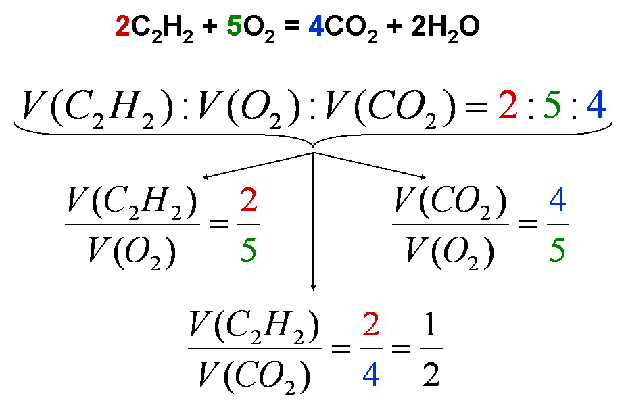
Задачи, решённые в классе
1. Аммиак горит в хлоре. Продукты горения — азот и хлороводород. В каких объемных соотношениях: а) реагируют при этом аммиак и хлор; б) получаются азот и хлороводород?
2. В каком объемном соотношении должны быть смешаны оксид углерода (II) и кислород, чтобы при поджигании газы полностью прореагировали? Каково соотношение объемов получившегося углекислого газа и исходной смеси газов при одинаковых условиях?
3. Сколько литров хлороводорода образуется при взаимодействии 6 л водорода с хлором?
4. Какой объём сероводорода получится при сжигании серы в водороде, объёмом 12 л?
5. Какой объём кислорода необходим для окисления 9 л оксида углерода(II) в оксид углерода(IV)?
Задачи для решения дома
6. Какой объём водорода требуется для получения 16 л аммиака?
7. Сколько литров оксида азота(II) потребуется для реакции с 3 л кислорода? NO + O2 →NO2.
8. Сколько литров водорода расходуется на получение 1 л аммиака?
9. Сколько литров кислорода расходуется на окисление 1 л аммиака по схеме реакции: NH3 + O2 →N2 + H2O.
10. Какой объём кислорода требуется для окисления 40 л аммиака по схеме реакции: NH3 + O2 →NO + H2O.
11*. Увеличивается, уменьшается или остается неизменным объем газов при сжигании серы в кислороде? Все измерения объема газов до и после опыта производятся при одинаковых условиях.
12*. Во сколько раз объем кислорода, вступающего в реакцию при окислении сероводорода H2S до оксида серы SO2 и воды, превышает объем сероводорода?
13*. При сжигании водорода в замкнутой системе в избытке кислорода объем газовой смеси после охлаждения до прежней температуры сократился на 27 мл. Каков был исходный объем водорода?
14*. 6 мл водорода сожгли в избытке кислорода. На сколько сократился объем газовой смеси после охлаждения ее до прежней температуры?
15*. В каком соотношении объемов должны быть смешаны метан CH4 и оксид углерода (II), чтобы для полного сгорания (до углекислого газа и воды) любого объема этой смеси расходовался такой же объем кислорода?
|
| темы уроков |
| тесты |
| готовимся к экзамену |
 |
 |
 |





